热力学第一定律(量子力学三大定律)
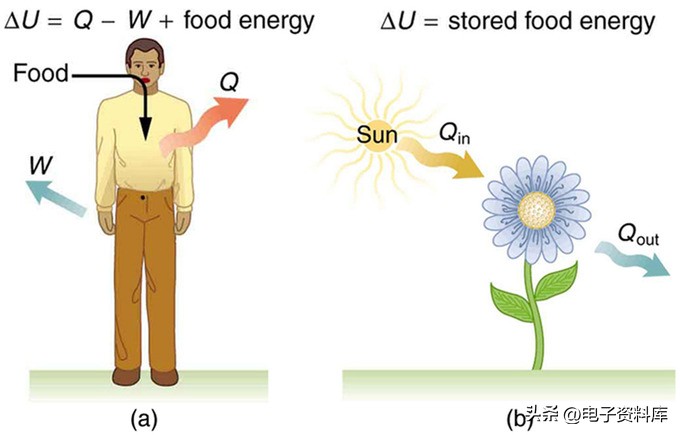
我们都生活在一个物质和能量不断交换的系统中;这是一个无穷无尽的流程。以吃饭的过程为例,你吸收食物的化学能,并将其转化为你的身体可以使用的形式。既然你的身体已经从食物中获得能量,它就可以在世界上进行锻炼了。
当系统释放热量或做某种功时,系统的内能会减少。同样,如果将热量添加到系统中,或者对系统做功,系统的内能也会增加。系统释放的任何一种能量都会被其周围环境吸收,而周围环境损失的任何一种能量都会被系统吸收。在所有这些例子中,你不是在创造或破坏能量;而是在创造能量。它只是从一个地方移动到另一个地方。用数学表示,这看起来像:
这种能量从一种状态转换到另一种状态的交换过程都发生在一组系统和环境中。当您早上打开电热水壶时,您的金属容器中装有水,这就是您的系统。厨房的其余部分,甚至房子的其余部分,都是周围的环境。
当您的茶壶开始沸腾时,它会将一些水转化为蒸汽,从顶部的壶嘴释放出来。这种转换后的能量从金属容器内的系统跨越边界到达其外部的环境。这是工作中的热力学,是系统和环境之间能量和物质的转移。
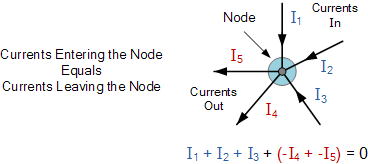
当与电子学相关时,热力学第一定律与基尔霍夫电流定律相似。这条著名的定律指出,进入节点的电流量等于离开节点的电流量。不管你有多少节点,进去什么,必须出来。
热力学第三定律说,在绝对零温度下完美的晶体结构将具有零无序或熵。但是,如果这种晶体结构中存在最微小的缺陷,那么熵也将是最少量的。不过,这条定律有点奇怪,因为即使在零开尔文时,仍然会发生一些原子运动,所以它有点理论化。无论如何,这条定律使我们能够理解,当系统的熵接近绝对零的温度时,系统中存在的熵会减少。
1850年,德国物理学家鲁道夫克劳修斯提出克劳修斯声明,称“热量通常不能自发地从较低温度的材料流向较高温度的材料”。大约在同一时间,威廉汤姆森(开尔文勋爵)制定了开尔文声明,其中说“不可能在循环过程中完全转换热量[不损失能量]。” 这两个陈述继续形成了热力学第一和第二定律的基础。热力学第三定律后来由德国化学家Walther Nernst开发,通常被称为 Nernst 定理。
系统是由观察者定义的,所以对于一个人来说,茶壶可能就是系统。对另一个人来说,整个房子可能就是系统,而邻居就是周围环境,这一切都取决于你的观点。关键是,热力学中的每个系统都包含在定义的边界内,而边界的另一侧是周围环境。热力学中存在三种类型的系统:
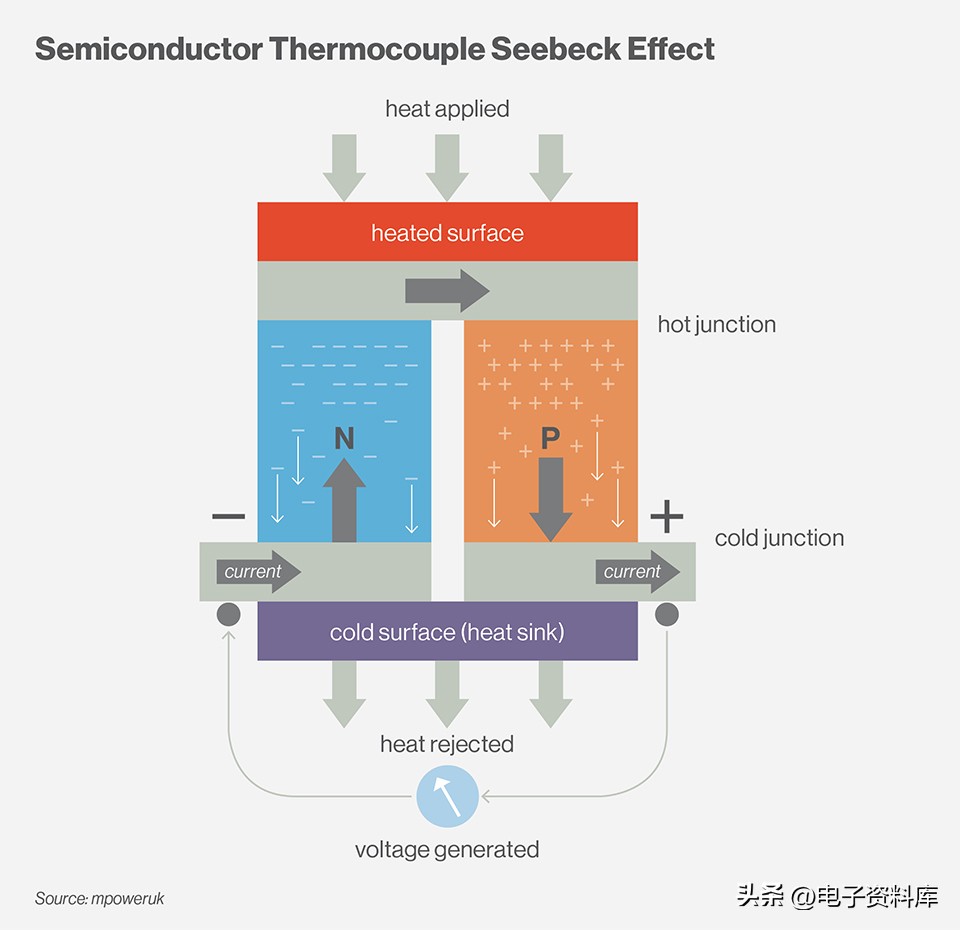
环顾四周,看看这个令人惊叹的运动能量世界,你会看到热力学定律在起作用。无论是在将食物的化学能转化为身体可用能量的过程中,还是在汽车或飞机中将机械能转化为动能的过程中。热力学是一种生活方式。您甚至会在您的电子设计中发现热力学定律。像基尔霍夫电流定律这样的原理与热力学第一定律完全一致,指出进入一组节点的电流必须出来,就像能量不能被创造或摧毁,只能被转化。对于热力学第二定律,我们在电路中观察到塞贝克效应,加热的电子器件将流向较冷的导体,并在此过程中在电路中产生电流。在这里,我们有熵在起作用,无论它走到哪里,都会产生越来越多的无序状态。
这里,宇宙内的总熵ΔS宇宙等于系统内的总熵ΔS sys加上所有周围环境的总能量ΔS surr,所有这些都不能小于0。为什么?因为在任何时候,一天中的所有时间,所有的能量都在从一种形式转变为另一种形式,其中一种形式是无法使用的能量。驾驶汽车使用机械能产生运动动能,但在此过程中,您还将大量能量转化为热量。这是不可避免的副产品。
第一定律包含三个相关的概念——功、热和内能。热量是两个系统之间的热能传递。功是在系统与其周围环境之间传递能量的力。通过在系统内或系统外产生功,您会产生热量。然后是内部能量,它是系统内的所有能量。当热、功和内能相互作用时,能量就会发生转化。您可以用数学方法将这种关系表示为:
这对我们的系统与环境之间的平衡方程来说是不是很熟悉?
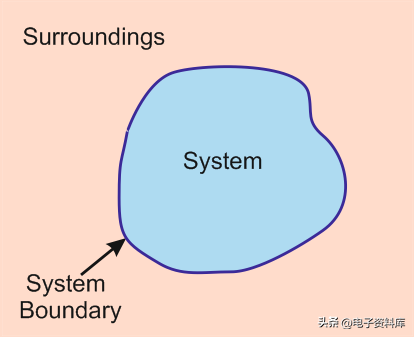

每个热力学系统都被边界和环境所包围。(图片来源)
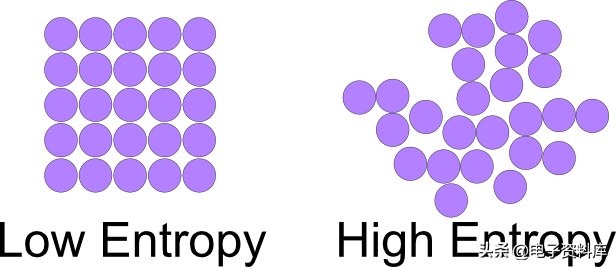
在这个拼图示例中,随机放置的拼图代表了更高形式的无序或熵。这就是为什么轮胎在被刺破时会释放空气,或者为什么在室温下放置的冰块最终会融化,或者为什么电路中的电子会从负极流向正极。当然,所有这些动作都有可能反过来发生,但是它们发生的概率很低,而且概率增加的牌堆得很高,以至于它们根本不会发生。
考虑熵的另一种方法是概率。以一个装满拼图的盒子为例。您将所有拼图块从盒子中倾倒出来,其中一个拼图随机落在它与另一块完美连接的地方的概率是多少?这是一个很小的概率。在同一个盒子里,一块随机落在它不适合另一块的地方的概率是多少?这是一个很高的概率。
一个开放系统,可以在系统与其周围环境之间交换能量和物质。一个封闭系统,其中只有能量可以在系统与其周围环境之间交换,而不是物质。一个孤立的系统,系统与其周围环境之间没有能量或物质交换。真正孤立的系统很少见。在高层次上,我们的整个宇宙被认为是一个系统,但我们宇宙的边界是什么,它的周围是什么?这些是我们尚未回答的一些更大的问题。对于电子设计师来说,热力学通过您设计的日常设备呈现出更加个性化的现实。您会发现,您已经使用的许多用于计算和分析电路(如基尔霍夫定律)的原理都是基于热力学的基础。
热力学定律不是一个人发现的。这一发展可以追溯到 1600 年代,当时热量和温度的基本概念首次被提出。1824 年,法国物理学家萨迪·卡诺 (Sadi Carnot) 在讨论理想机器的效率时率先定义了热力学的基本原理。萨迪最初使用热量系统来描述发动机运动过程中损失的热量,后来在热力学第二定律中被熵取代。
这里,ΔU是系统内部能量的总变化,Q是系统与周围环境之间的热交换,W是系统所做的功。
热力学第二定律,也称为熵增定律,指出随着时间的推移,系统中的无组织状态或熵总是会增加。这是什么意思?举个例子——为什么你的办公桌总是随着一周的进展而变得更乱?或者更重要的是,为什么你的办公室不用你自己动手就可以从凌乱到干净?这是热力学中的时间箭头。随着时间的增加,混乱也会增加。
这里,ΔU s系统是系统中的总内能,并且总是等于周围环境中的总能量的ΔU 。
无论你在设计什么,你都在根据热力学定律进行设计。将这些原则付诸实践,
如果系统 A 与系统 C 平衡系统 B 与系统 C 平衡那么系统 A 和系统 B 也处于平衡状态。该定律允许您定义系统之间的热流方向。如果您知道一组连接系统的温度,那么您将根据热平衡的基本原理知道热量将向哪个方向传播。
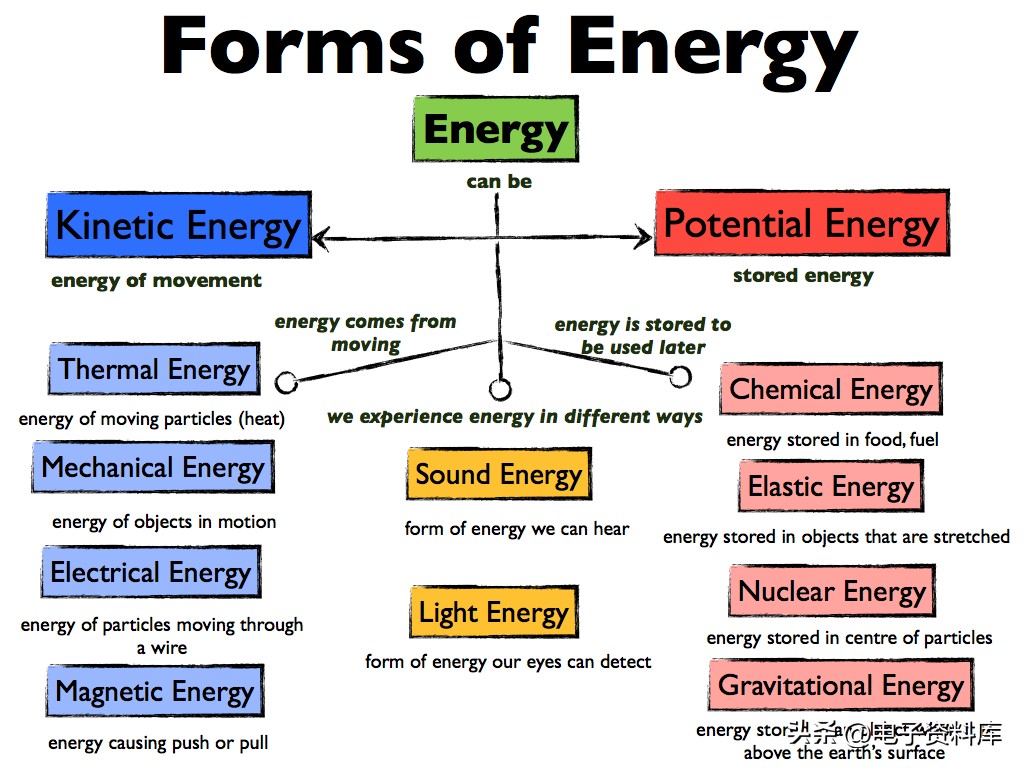
热力学第一定律,也称为能量守恒定律,说能量不能被创造或毁灭,它只能改变形式。能量有很多不同的形式,包括:
在下图中,我们有两个电流进入节点,三个电流离开节点。根据基尔霍夫电流定律,电流进出节点之间的关系可以表示为:
关于第一定律要记住的重要一点是,能量的转换并不是 100% 有效的。在我们的灯泡示例中,您可以将电能转换为可用的光能形式,但在此过程中,您会以热的形式产生不可用的能量。
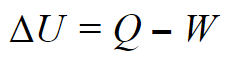

请注意,虽然我们最后介绍的是第零定律,但它实际上是第一位的。在 18 世纪定义热力学定律时,只包括前三个。然而,科学家们意识到他们需要定义温度运动的第四定律。英国科学家罗伯特·福勒(Robert Fowler)没有对所有现有法律重新编号并给现有文献增加混乱,而是提出了第零定律这个名字。

在电子学中,我们看到热力学第二定律与塞贝克效应一起起作用。当热量施加到两个导体之一时会发生这种现象,这会导致加热的电子流向较冷的导体。如果将这对加热导体在电路中连接在一起,则加热效应将导致直流电 (DC) 流过电路。在这种情况下,冷导体中处于较低熵状态的电子通过加热达到较高的熵状态,因此无序性增加。
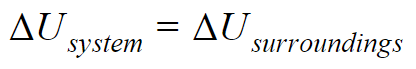
一切都是热力学。这不仅仅是为物理学领域保留的概念,也不是您只能在电子产品、冰箱、汽车、飞机等中找到的一套定律。这是一个将自身编织到织物中的科学概念的生活。问题是,热力学只是能量的工作方式,所以很容易被忽略。当您一周又一周地打扫办公室时,似乎一天比一天更乱,这就是热力学第二定律在起作用,所有事情都会导致混乱状态加剧。或者当你这个周末在烤架上烤出美味的牛排时,这就是热力学第一定律在起作用,以热量的形式将能量传递给你的食物。热力学不仅仅是对热和功的研究;这是对能量如何的研究,热力学是对生命的研究。
这种现象发生在任何系统中。随着时间的推移,可用能源最终将让位于不可用能源。虽然根据第一定律不能创造或破坏能量,但它可以从有用的状态变为不太有用的状态,如热能(热量)。
热力学第零定律说,如果两个系统与第三个系统处于热平衡状态,那么前两个系统也彼此处于热平衡状态。使用我们古老的等式传递属性:
在我们的灯泡示例中,我们将灯泡打开的时间越长,将电能转换为辐射能,我们继续以热的形式将更多的可用能量转换为不可用的能量。随着系统内可用能量的减少和不可用能量的增加,我们说系统的熵增加了。数学上说:
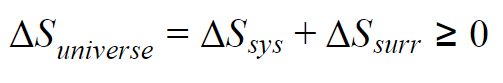

能量不会被创造或毁灭;它只是从一种形式变为另一种形式。打开电灯开关不会产生能量,它只是将电能转换为辐射能(光)和热能(热)。
印度疫情为何突然消失 朝鲜内乱最新消息
疫情三年,我们的措施在不断优化,时至今日,放开的呼声越来越高。确实,所有人都感觉到有些疲惫了,三年来,收入下降,出行不便等诸多因素,让越来越多的人感到压抑。许多国家在疫情早期,采取的措施跟我们差不多,但很快他们就决定要跟病毒共存,在那时的我们看来,他们的做法简直不可思议。印度疫情早期大财经2023-03-22 01:24:300001花五十万能建一个多大规模的充电站,盈利每天能有多少?
大家好,我知道很多人都在关注投资新兴行业,都想在新兴行业里分一杯羹,最近这几年新能源行业崛起的是相当迅猛,伴随新能源汽车的崛起,随之其上下游都跟着过起了小康生活,今天咱们分享一个花五十万就能做的朝阳行业,这个行业为啥很多人抢着做,带你来看看他的盈利手段有哪些:一、国家、地方补贴:1.一次性设备补贴(个别地区是整个充电站投资的30%)2.电价补贴,一度电会给你补贴0.5-0.8毛钱。大财经2023-10-25 15:08:330000景点门票未用却不可退?五一假期这些消费投诉较集中
上海市市场监管局5月3日透露,2023年五一假期,市市场监管局12315热线平台共接收投诉举报和咨询37705件,其中投诉举报21637件、咨询16068件。从投诉举报涉及行业看,食品(2952件)、服装鞋帽(2892件)、家居用品(1678件)、餐饮住宿服务(1356件)、文化娱乐和体育服务(1116件)等投诉举报量居前。分析假日期间投诉举报,主要呈现“三个集中”:0000两个浙江人做矿泉水,一个公司上市成首富,一个却30年坚持不上市
2020年9月,股市迎来一阵沸腾之势,所有购买了农夫山泉股票的股民们,纷纷感叹自己眼光独到。因为这个占据着中国大半市场份额的矿泉水企业,宣布在香港挂牌上市。随着这一消息的发出,其创始人钟睒睒的身家估值已经超过5000亿,成为名副其实的中国首富。不少浙江人认为,这位优秀的企业家为家乡增了光,与此同时,他们也联想到了另一位同样做白水生意的企业家。两个人虽然同样来自浙江,事业轨迹却完全不同。大财经2023-11-09 16:57:110000